NUMERO DE OXIDACIÓN
- Elnúmero de oxidación es un número entero que representa el número de electrones que un átomo recibe (signo menos) o que pone a disposición de otros (signo más) cuando forma un compuesto determinado.
- Eso significa que el número de oxidación es positivo si el átomo pierde electrones, o los comparte con un átomo que tenga tendencia a captarlos. Y será negativo cuando el átomo gane electrones, o los comparta con un átomo que tenga tendencia a cederlos
J
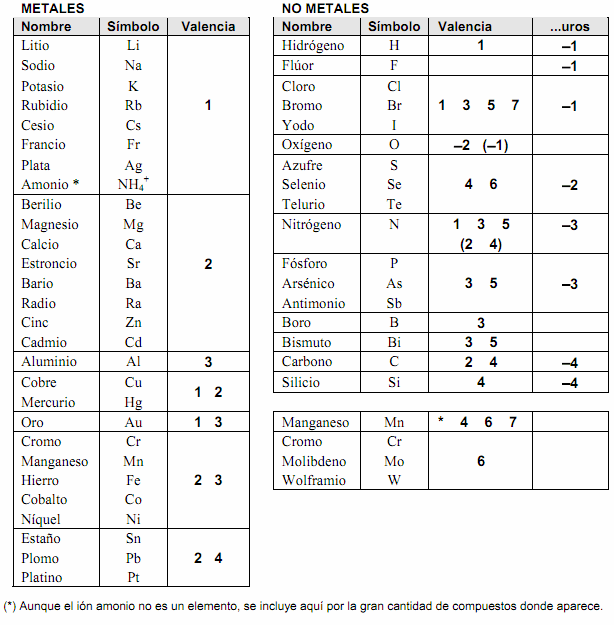
TABLA DE VALENCIA DE LOS ELEMENTOS QUIMICOS
COMPUESTO
Un COMPUESTO es
una sustancia formada por la unión de dos o más elementos de la tabla
periódica. Una característica esencial es que tiene una fórmula química. Los compuestos químicos son aquellas sustancias que
están compuestas por la unión de al menos dos elementos incluidos en la tabla
periódica. Los compuestos químicos pueden ser clasificados en los siguientes
grupos:
Óxidos Básicos:

COMPUESTOS BINARIOS
Utilizan dos tipos de elementos
OxigenadosÓxidos Básicos:
Son
compuestos con elevado punto de fusión que se forma como consecuencia de
la reacción de un metal con él oxígeno. Esta reacción es la que produce la corrosión de los metales al estar expuesto al oxigeno del aire.
¿Cómo se formulan?
Los óxidos tienen la siguiente formula, que se aplica a todas las combinaciones: X2On, donde X es el símbolo del elemento, el 2 corresponde a la valencia del oxígeno, la O es el símbolo del Oxígeno y la n es la valencia del elemento metálico.
Los óxidos tienen la siguiente formula, que se aplica a todas las combinaciones: X2On, donde X es el símbolo del elemento, el 2 corresponde a la valencia del oxígeno, la O es el símbolo del Oxígeno y la n es la valencia del elemento metálico.
Formulación: Metal + oxígeno = óxido básico
Oxidos Ácidos:
Son los
óxidos de los no metales. Producto formado por una combinación del oxígeno con
un elemento no metal y que, al reaccionar con el agua, da un ácido.
Cuerpo que procede de la deshidratación de los
ácidos o de la combinación del oxígeno con los elementos metaloides. Los óxidos
de elementos más electronegativos tienden a ser ácidos. Se llaman anhídridos
ácidos; agregando agua, forman oxácidos.
Por ejemplo, el heptaóxido de dicloro es ácido; el
ácido perclórico es una forma hidratada. Cuerpo que procede de la
deshidratación de los ácidos o de la combinación del oxígeno con los elementos
metaloides. Carbónico. Gas asfixiante y no combustible que se forma por la
combinación del carbono con el oxígeno.
Formulación: No Metal+Oxigeno = Anhídridos

Hidrogenados
Hidruros:
Formulación: Metal+Hidrogeno = Hidruros.

Formulación: Hidrogeno+No Metal = Hidráciodos(f1,f2).

No Metal de la familia(f3yf4)+Hidrogeno = compuesto especial
NH3 Amoniacos
PH3 Formina
AsH3 Arsina
SbH3 Estirbina
BH3 Borato
GeH4 Germano
CH4 Metano
SiH4 Silano
Sales Binarias y Halogrnas
Metal+No Metal = Sal Binaria
M + NM formulación N.tradicional N.sistematica
Hidruros:
Son compuestos binarios formados por
la combinación de metal e hidrógeno actúa con número de oxidación -1.
Por lo general son sólidos, sin embargo, si se disuelven en agua, forman iones.
Por lo general son sólidos, sin embargo, si se disuelven en agua, forman iones.

Hidrácidos:
Un hidrácido es un ácido que no contiene oxígeno
sino que son compuestos binarios formados por un no metal (halógeno) e
hidrógeno, y son los más simples. La nomenclatura diferencia las sustancias
gaseosas de sus soluciones ácidas.

Compuestos Especiales:
NH3 Amoniacos
PH3 Formina
AsH3 Arsina
SbH3 Estirbina
BH3 Borato
GeH4 Germano
CH4 Metano
SiH4 Silano
Sales Binarias y Halogrnas
Metal+No Metal = Sal Binaria
M + NM formulación N.tradicional N.sistematica
Na1+Cl1 = NaCl Cloruro de sodio monocloruro de sodio
Fe3+S2 = Fe2S3 Sulfuro ferrico trisulfuro de dihierro
Mg2+N3 = Mg3N2 Nitruro de magnecio dinitruro de trimagnecio
Be2+Br1 = BeBr2 Bromuro de berilio dibromuro de berilio
Li1+Se2 = Li2Se Selenuro de litio monoselenuro de dilitio
Ca2+C4 = Ca2C Carbonuro de calcio monocarbonuro de dicalcio
COMPUESTOS TERNARIOS
Utilizan tres tipos de elementos
Hidroxidos (Bases):
Los hidróxidos están formados por el grupo OH-, que actúa con número de oxidación -1, y un metal.
Para formular: escribe el símbolo del metal seguido del OH, entre paréntesis, e intercambia los números de oxidación como subíndices sin signo. Si el subíndice del grupo OH es 1 no se escribe el paréntesis.
Para nombrar: utiliza el mismo procedimiento que en los compuestos binarios. Empieza con "hidróxido de", seguido del nombre del metal y utiliza los prefijos numerales o el sistema de Stock.
Formulación: Metal+(OH) = Hidroxido
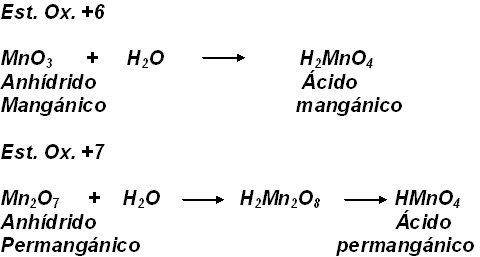
Oxacidos (Acidos):
Son compuestos ternarios formados por hidrógeno, oxígeno y un no metal.
La nomenclatura tradicional es la más utilizada en los ácidos habituales. Al no existir una regla estricta para nombrarlos es mejor que te los aprendas.
Formulación: Anhidrido+H2O = Oxacido
SO3 (s)
+ H2O(l) = H2SO4 (ac)
N2O5 (g) + H2O(l)
= 2HNO3 (ac)
P4O10 (s) + H2O(l)
= 4 H3PO4 (ac)

Sales Ternarias:
Oxacido+Hidróxido = sal neutra + agua.
COMPUESTOS CUATERNARIOS
Utilizan cuatro y cinco tipos de elementos.
Sales Oxisales Basicas:
Acidos ternarios+hodroxidoscon mas de 2(OH) = M(OH) NM+H2O.
Sales Oxisales Acidas:
Acidos ternarios con mas de 2H+hidracidos = MH NM+H2O.
Sales Oxisales Dobles:
Acidos ternarios con mas de 2H+2hidroxidos metales diferentes = M M NM+H2O.
Sales Oxisales Mixtas:
Acidos ternarios diferentes+hidroxidos con mas de 2(OH) = M NM NM+H2O.
Prefijos y sufijos de la nomenclatura tradicional












0 comentarios:
Publicar un comentario